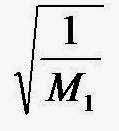DISTRIBUSI
KECEPATAN PARTIKEL GAS IDEAL.
Dalam gas
ideal yang sesungguhnya atom-atom tidak sama kecepatannya. Sebagian bergerak
lebih cepat, sebagian lebih lambat. Tetapi sebagai pendekatan kita anggap semua
atom itu kecepatannya sama. Demikian pula arah kecepatannya atom-atom dalam gas
tidak sama. Untuk mudahnya kita anggap saja bahwa : sepertiga jumlah atom
bergerak sejajar sumbu x, sepertiga jumlah atom bergerak sejajar sumbu y dan
sepertiga lagi bergerak sejajar sumbu z.
Kecepatan
bergerak tia-tiap atom dapat ditulis dengan bentuk persamaan :
vras = kecepatan tiap-tiap atom,
dalam m/det
k =
konstanta Boltzman k = 1,38 x 10-23
joule/atom oK
T = suhu
dalam oK
m = massa
atom, dalam satuan kilogram.
Hubungan
antara jumlah rata-rata partikel yang bergerak dalam suatu ruang ke arah kiri
dan kanan dengan kecepatan partikel gas ideal, digambarkan oleh MAXWELL dalam bentuk : DISTRIBUSI MAXWELL.
M = massa
gas per mol dalam satuan kg/mol
R =
konstanta gas umum = 8,317 joule/moloK
Dari
persamaan di atas dapat dinyatakan bahwa :
Pada suhu yang sama, untuk 2 macam gas kecepatannya
dapat dinyatakan :
vras2 = kecepatan molekul
gas 2
M1
= massa molekul gas 1
M2
= massa molekul gas 2
Pada gas yang sama, namun suhu berbeda dapat
disimpulkan :